pH, Su Değerleri ve İyon Gereksinimleri
Herkese merhabalar. pH ve su
değerleri hakkında edindiğim bilgileri sizlerle paylaşmak isterim. Zira su ve
iyonlar arasındaki ilişki ile alakalı bilgiler dağınık vaziyette ve bu durum
bilgi kirliliği yaratmakta. Öncelikle suyun asitliği ve bazlığı ile ilgili
bilgiyi öğrendiğimiz parametreyle, pH ile başlayalım.
pH
pH, suyun asitlik-bazlık
durumunu belirten parametredir. Bilindiği üzere saf su tam olarak 7 pH'a
sahiptir ki, bu asitlik ve bazlığa eşit mesafede olduğunu yani nötr olduğunu
belirtir. 7’den küçük olan bütün pH değerleri asidik, 7’den büyük olan bütün pH
değerleri de bazik olarak adlandırılır. Peki bu sayılar nasıl hesaplanır ve ne
anlama gelmektedir?
İlk olarak saf suyun
kimyasını, detaylı olarak ele alalım:
Su, H2O moleküllerinden oluşmaktadır. H2O
suyun kararlı formudur ve çok çok büyük kısmı, kararlı olan bu halde
bulunmaktadır. Bunun yanı sıra, aynı zamanda 2 su molekülü etkileşerek, H3O+ ve OH- iyonlarını da oluşturur. H3O+ asitliğe neden olurken, OH- bazlığı oluşturan iyondur. Saf su içinde 2 iyon bir
araya gelip, birer birim H3O+ ve OH- iyonu oluşturacağından, bu iyonların
konsantrasyonu eşit ve 10-7 şer molar olarak
dengelenmektedir. Ayrıca, konsantrasyon değerleri değişiklik gösterse bile her
zaman bu iki iyonun konsantrasyon çarpımı 10-14 değerine eşit
olacaktır. (molar terimi, çözelti konsantrasyonunu belirtmek için kullanılır ve
Molar=mol/litre formülü ile bulunur).
Peki saf su için 7 sayısı nereden
gelmektedir? Asitliği daha kolay ifade etmek için, konsantrasyon değeri, pH
olarak yeniden formüle edilmiş, bunu yaparken de “-log(H3O+ konsantrasyonu)” formülü kullanılmıştır. Saf
su için, asitlik konsantrasyonunu formülde yerine koyduğumuzda, pH=-log(H3O+)=-log(10-7)=-(-7log10)=7*1=7
olarak karşımıza çıkmaktadır.
Saf suda herhangi başka bir iyon
bulunmadığından ve saf su yalnızca kendi molekülleri ile etkileşimde
bulunabileceğinden pH her zaman sabit ve 7 değerindedir. Peki suda başka
iyonlar da bulunursa veya iyon eklemesi yapılırsa pH değişir mi? İyon türüne
göre farklılık göstermekle beraber, genel olarak pH değişmektedir. Ancak formül
aynıdır ve asit konsantrasyonu ne olursa olsun, H3O+ ve OH- iyonlarının konsantrasyon değerlerinin
çarpımı 10-14 değerine eşit olacaktır. Bu noktada, pOH
terimini de açıklayayım. pOH, pH’a benzer şekilde hesaplanmakla birlikte,
bazlık değerini simgelemektedir. Nasıl pH hesabında, asitliği oluşturan H3O+ konsantrasyonunu formülde yerine koyduysak,
pOH için de OH- iyonu konsantrasyon değerini, “-log(OH- konsantrasyonu)” formülünde yerine koyacak ve pOH
değerini bulacağız. pH ve pOH arasında sabit bir ilişki vardır ve birbirlerine
dönüştürmek için; pH=14-pOH veya pOH=14-pH formülleri kullanılır.
Örneklemek gerekirse; saf su için pH=7 ve
pOH=14-7=7 dir. Yukarıda belirtildiği gibi, iki iyonun konsantrasyon çarpımları
sabit ve “p” dönüşümü ile toplam 14’e eşittir. Benzer şekilde aşağıdaki
örneklerde asitlik ve bazlık ilişkilerini görebiliriz:
A: pH=3, pOH=14-3=11 Asidik çözelti
B:
pH=2.87, pOH=14-2.87=11.13 Asidik çözelti
C:
pH=8.17,
pOH=14-8.17=5.83 Bazik
çözelti
D:
pH=4.5,
pOH=14-4.5=9.5
Asidik çözelti
E:
pH=7.6,
pOH=14-7.6=6.4
Bazik çözelti
.. …………….
…………………………..
……………………
..
……………. ………………………….. ……………………
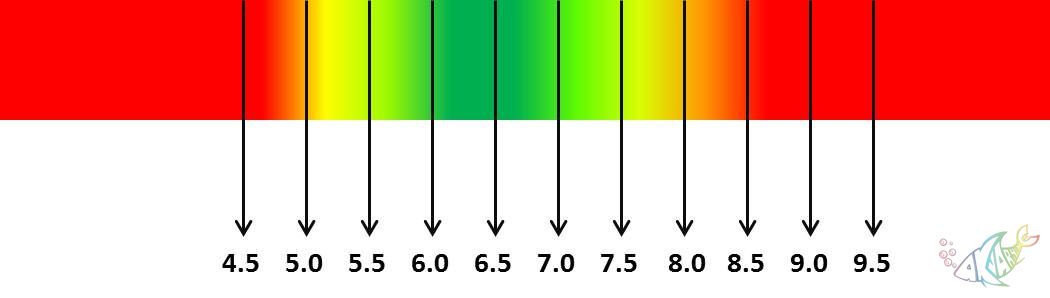
Akvaryum hobisinde çoğunlukla pH terimini kullandığımızdan, bu noktadan itibaren pH üzerinden devam edeceğiz. Terimsel olarak, 7’den büyük pH değerleri bazik, 7’den küçük pH değerleri asidik çözelti oluşturur demiştik. Peki akvaryumlarda pH sınır değerleri nedir? Akvaryum suyumuz ne kadar asidik veya ne kadar bazik olabilir? Canlıların ve bitkilerin tolerans sınırları nelerdir? Aşağıdaki grafiklerde, tatlı su akvaryumları için optimum pH değerleri belirtilmiştir.
Grafik 1. Bitkili akvaryumlar için uygun pH değerleri grafiği
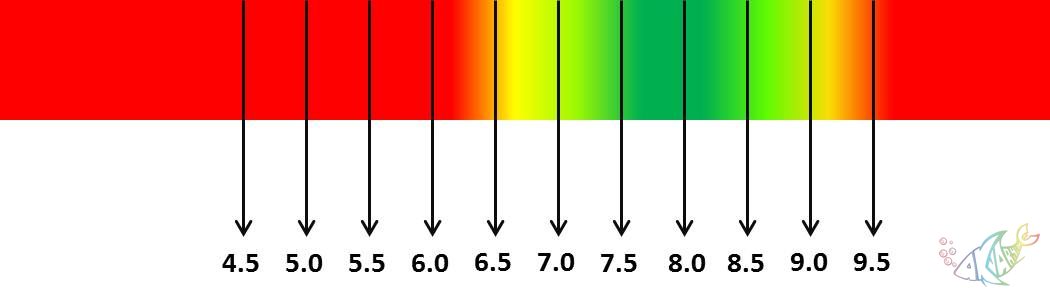
Grafik 2. Mineralli su (Malawi-Tanganyika) akvaryumları
için uygun pH değerleri grafiği
Bitkili akvaryumlar için Grafik 1’de gözlenen
yeşil pH değerleri en uygun değerlerdir. Kırmızı renk arttıkça risk ve zarar
artacaktır. Bitkili akvaryumlardan kasıt, yumuşak su, yani kıyasla asidik ve
fazla iyon içermeyen su değerlerinin uygun olduğu akvaryumlardır. Bu gibi
akvaryumlarda bitki türleri ile birlikte, amazon balıkları (Discus, tetralar,
ramirezi, melek, vs.), canlı doğuranlar, sazansıgiller, kedi balıkları,
omurgasızlar (kerevitler, karidesler, yengeçler, salyangozlar, vs.) ve daha pek
çok tür canlı beslenebilir. Bu gibi canlılar, doğal habitatlarında nehir
kaynaklı sular içinde yaşadıklarından, yüksek iyonlu ve/veya bazik sulara
uyumlu değillerdir. Aynı şekilde Malawi ve Tanganiya çikletleri de habitatları
gereği yüksek pH ve sertlikte sulardan hoşlanırlar. Peki neden? Bu noktada,
doğal habitatlarda neden su değerlerinde farklılıklar olduğunu ele alalım.
Su ve iyon ilişkisini ele alırken, ilk olarak
çok duyular genel sertlik (general hardness (GH)), karbonat sertliği (carbonate
hardness (KH)), toplam çözünmüş katılar (total dissolved solids (TDS)),
milyondaki parça (parts per million (ppm)) sert su, yumuşak su, ters ozmos
(reverse osmosis (RO)) gibi terimleri açıklayalım. Açıklamalar sonrasında
detaylı olarak ilişkilendirme yapacağız.
Genel Sertlik (GH)
Genel sertlik, GH kısaltması ile ifade edilen
ve su içinde çözünmüş bütün iyonları hesaba dahil eden terimdir. Su içindeki
tortu ve iyonlar toplamı bu terim ile ifade edilir. Genel sertlik, yağmur
suyunun toprak ile etkileşimi sonucu içerisinde iyonlar çözmesi ile veya
tortuların su içinde askıda kalmasıyla oluşur. Bunun yanında göl suları,
çoğunlukla yeraltı sularından beslendiğinden, yeraltında tuzları bakımından
zengindir. Çünkü kaynak suları yüzeye hareket sırasında güzergahı üzerinde bulunan
tuzları çözer ve birikintiye taşır. Deniz suyu için ise durum hepsinin toplamı
olarak düşünülebilir. Ayrıca denizlerde buharlaşma oluştuğundan, iyon yoğunluğu
da dünyanın oluşumundan bu güne artarak doygun hale erişmiştir. Denize erişen
her türlü yüzey ve yeraltı suyu bir takım iyonları denize taşır. Denizden de
buharlaşma eseri sürekli saf su çıkışı olur. Buharlaşan saf su yoğunlaşıp dünya
yüzeyine erişip, iyon toplayarak tekrar denize karışır. Tüm bu döngü eseri
yeryüzünde veya yeraltında bulunan mineraller denizlere taşınır. Bu sebeptendir
ki, deniz suyu sertliği 6600ppm civarındadır. Nehir suyu genel sertliği
değişmekle birlikte 0-375ppm iken, göl suları yeraltı kaynaklarından beslendiği
için 0-1000ppm arası değerlere sahiptir. Nehir ve göl sularının GH değerlerinin
geniş aralık bulundurması coğrafi etkilerden kaynaklanmaktadır. Yaşlı bir nehir
deltası mineralleri milyonlarca yıl süpürür ve denize taşırsa, çözebileceği az
miktarda alüvyon kalacağından düşük GH değerine sahip olabilecekken, kıyasla
genç bir delta zengin alüvyon içeriğinden dolayı yüksek GH değerine sahip
olabilir. Genel sertliği azaltmak için suyu havalandırmak (şebeke sularına
eklenen klorun gaz haline dönüşüp uçurulması için), su arıtıcıları kullanmak
(genellikle tortu ve renk verici organik maddeleri süzer) veya ozmos filtreler
kullanmak (aşağıda detaylı olarak açıklayacağız) yararlı olur. İhtiyaca göre
başka metodlar geliştirilebilir veya uygun metod seçilebilir.
Karbonat Sertliği (KH)
Karbonat sertliği ise KH kısaltması ile ifade
edilen ve su içinde yalnızca çözünmüş karbonat ve bikarbonat iyonlarını hesaba
dahil eden terimdir. Çok yoğun su döngüsüne maruz kalan habitatlarda karbonat
sertliği düşük olacaktır. Buna karşılık birikintilerde KH değerleri yüksek
olacaktır. Sebep açıktır; yüksek su döngüsü bulunan deltalarda iyonlar bir
şekilde taşınır. Bunu yıkamak olarak düşünebilir. Sınırlı miktarda mineral
içeren deltalarda, yüksek debili nehir akıntıları mineralleri yıkayarak denize
ulaştıracaktır. Ancak göllerden yalnızca buharlaşma ile su hareketi
oluşacağından, iyon miktarları yeraltı su kaynakları dolayısıyla bellir bir
noktaya kadar artış gösterecek ve sabitlenecektir. Bu yüzden göl suları sodalı,
yani karbonatlı olarak bilinir. Canlılar da habitatları icabı karbonata
mukavemet gösterebilir. Amazon nehrinde su çok az iyon içerdiğinden, amazon
canlıları düşük KH tercih edeceklerdir. Benzer şekilde kristal karideslerin
doğal habitatları, asyanın yüksek yağmur alan nehirleri olduğundan ve bu sular
mineral içermeyecek kadar yumuşak olduğundan bu canlılar karbonata tahammül
edemezler. Karbonat sertliğini azaltmak için ozmos filtre en uygun metottur.
Suyu kaynatarak karbonatı karbondioksite çevirerek de KH azaltılabilir ancak bu
teknik, akvaryum kullanımında çok verimli olmayacaktır. Çünkü suyu kaynatmak
muazzam enerjiler gerektirecek ve bu durum çok masraflı olacaktır.
Toplam Çözünmüş Katılar
(TDS)
Genel sertlikle aynı olmakla birlikte ifade
ediliş şekli farklılık gösterir. Suda çözünen tüm iyon ve katıları kapsar.
Milyondaki Parça (ppm)
İngilizcesi “parts per million” olan ve bir
milyon çözücü içinde kaç parça çözünenin olduğunu ifade eden terimdir. Hem GH
hem de KH değerlerini ifade etmek için kullanılabilir. 1ppm, 1mg/l olarak ifade
edilir. Örneklemek gerekirse, TDS değeri 200ppm olan bir akvaryum suyunda litre
başı 200 miligram çözünmüş iyon/tortu bulunmaktadır. Litre olarak ele alırsak,
100 litre ise akvaryum, toplamda 200mg*100litre=20 gram su haricinde çözünmüş
iyon/katı bulunur. Aynı şekilde ozmos filtre örneği verelim. Diyelim ki ozmos
filtrenizden 6ppm su çıkışı alıyorsunuz. Bu litre başı 6 miligram iyon
bulunduğunu işaret eder. 100 litre için de 6mg*100litre=600 miligram bulunur.
Tekrar belirtelim, ppm litre başı değerdir. Eğer akvaryumunuzda 200ppm değerini
okuyorsanız, bu 200mg/litre değeridir.
|
|
GH |
KH |
TDS |
|
GH |
1 |
- |
17.85ppm |
|
KH |
- |
1 |
17.85ppm |
|
TDS |
0.056 |
0.056 |
1 |
Tablo 1. TDS, GH ve KH arasındaki ilişki tablosu
Sert Su
İçinde çok yüksek miktarda iyon, tortu vs
içeren sudur (≥375ppm). Göl suları sert su olarak ifade edilebilir. 375ppm
altı, akvaryumlar için kabul edilebilir derecede yumuşak olarak kabul
edilebilirken, 375ppm üzeri sert olarak kabul edilmektedir.
Yumuşak Su
İçinde düşük miktarda iyon, tortu vs içeren
sudur (≤375ppm).
|
Derece |
Ppm cinsinden değer |
GH değeri |
|
Yumuşak |
0-100ppm |
0-5.6 |
|
Orta Sert |
100-375ppm |
5.6-21 |
|
Sert |
375-800ppm |
21-45 |
|
Çok Sert |
800+ ppm |
45+ |
Tablo 2. Akvaryum canlıları için su sertliği değerleri tablosu
Ters Ozmos (RO)
Ozmos, yüksek iyon konsantrasyonlu bir
ortamın, çevresindeki düşük iyon konsantrasyonu bulunan bir ortamdan su alarak
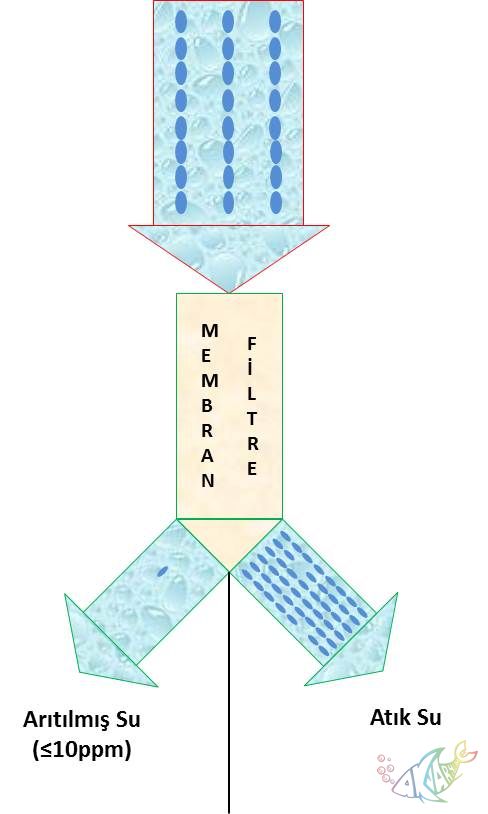
şişmesidir kısaca. Ters ozmos için ise bu durum tam terstir. Bir membran filtre
kullanılarak su iki parçaya ayırılır ve belli miktarda iyon içeren su iki
parçaya ayırılır. Bu parçaların biri saf suya yakın derecede az iyon içerirken
(maksimum 10ppm), diğer parça ilk değerin iki katı civarında iyon içerir.
Grafik 3. Ozmos filtrenin basitleştirilmiş çalışma
prensibi
Su Değerlerinde
Değişiklikler Yapmak
pH’ı Artırmak veya Azaltmak
pH’ı Artırmak
Akvaryum suyumuzun pH değerini artırmak
istiyorsak yani suyumuzu daha bazik hale getirmek istiyorsak yapacağımız şey
suya baz çözeltisi eklemek olacaktır. Bunu yaparken elimizde kesinlikle pH
değişimlerini takip edebileceğimiz bir pH metre olmalı. pH kağıtları da yararlı
olabilir ancak hassasiyet bakımından düşük olduklarından pH metre kadar iyi
sonuç vermeyeceklerdir. Sonuç olarak bir şekilde pH değişimlerini takip etmek
durumundayız. Bu noktada 2 farklı durum için pH artırmayı ele alacağız.
1.Bitkili akvaryum/Asidik su canlıları
akvaryumunda pH beklediğimizden çok düşük ise:
Aşırı miktarda karbondioksit eklenmesi veya suya salınım yapan bir malzeme dolayısıyla akvaryum suyumuzun pH değeri aşırı düşebilir. Bu durumda pH metre ile takip ederek suya damla damla baz çözeltisi eklemeliyiz. Eklemeleri yavaş ve aralıklı yapmak pH metrenin değişimleri takip etmesine yardımcı olacaktır. Peki baz çözeltisini nereden bulacağız veya hazırlayacağız? Bunun için sodyum hidroksit (NaOH) veya ihtiyaca göre potasyum hidroksit (KOH) uygun olacaktır. Eğer imkanımız var ise ve akvaryumumuz bitkili ise potasyum hidroksit, potasyum sağlaması açısından daha uygundur. Fakat sonuçta pH ayarlayacak kadar düşük miktarda ekleme yapacağımızdan ve bulunabilirliği daha kolay olduğundan sodyum hidroksit de işimize yarayacaktır. Her iki tür içinde yapacaklarımız aynı olacağından sodyum hidroksit üzerinden yazıya devam edeceğim. Marketlerde satılan lavabo açıcılar (Mr. Muscle, Bim lavabo aç, vs.) katı sodyum hidroksitten oluşmaktadır. Açık havada ve deriyle temas ettirmeden, soğuk suyla dolu 500ml bir pet şişeye yarım paket kadar lavabo aç eklenerek stok çözelti hazırlanır. Bu çözelti aşındırıcıdır ve 5-10 günden uzun süre saklanmamalıdır. Kesinlikle göz ve deri ile temasından sakınılmalıdır. Temas halinde ise, sirekeli su ile temas eden bölge yıkanmalıdır (göz hariç. Gözle temas halinde acilen hastaneye başvurunuz). Hazırlanan stok çözelti, bir damlalık kullanılarak yavaş yavaş ve pH metre ile takip edilerek akvaryuma eklenir. Her 10 damlada bir 20-30 saniye ara verip pH’ın dengelenmesi beklenmelidir. Arzu edilen pH değerine ulaştığınızda, izleyen birkaç gün pH’ı takip ediniz. Bir kez dengelendiğinde, yoğun su değişimleri yapmadıkça veya suya salınım yapan bir etken olmadıkça pH sabit kalacaktır. İlk bakışta korkutucu bir süreç olarak gözükse de, özenli ve dikkatli bir şekilde gerçekleştirildiğinde zararsız olarak pH ayarlanabilmektedir.
1.Malawi-Tanganyika Çikletleri için şebeke
suyu pH’ını yukarı çekmek:
İlk maddede açıklanan prosedür bu durum için de aynen geçerlidir. İlkinden farklı olarak, bu madde için karbonat kullanarak da pH ayarlaması yapılabilir. Yumuşak su canlılarının bulunduğu akvaryumlarda karbonat kullanımı sorunlar çıkarabildiği için karbonat kullanımını tavsiye edilmemektedir. Ancak çiklet akvaryumlarında karbonat kullanımı sorun çıkarmayacaktır. Kullanıma gelirsek, suya yavaş yavaş ve pH metre ile takip ederek karbonat eklenir. Eklenecek karbonat, litre başı 70-80 miligrama kadar kabul edilebilecektir. Eğer hala arzu edilen değerler gözlenemediyse, NaOH çözeltisiyle ph yükseltmeye devam edilebilir. Çiklet akvaryumlarında karbonat kullanılmasının bir diğer yararı ise, tampon kapasitesi oluşturularak pH değerinin değişiklik göstermesinin engellenebilmesidir. Tampon kapasitesi oluşturabilen iyonlar karbonat, sülfat, fosfat gibi iyon kökleridir. Bu gibi iyonlar, suda yeni oluşan/oluşabilecek asit ve baz iyonlarıyla etkileşimde bulunarak pH değişikliklerinin önüne geçerler. Saf suya bir damla limon suyu eklendiğinde, pH’ta 100 birim değişiklik oluştuğunu kabul edersek, yüksek tampon kapasitesine sahip bir suda aynı miktarda limon suyu belki 0.01 birim değişiklik oluşturabilir.
pH’ı Düşürmek
Akvaryum suyumuzun pH değerini düşürmek istiyorsak, yani
suyumuzu daha asidik hale getirmek istiyorsak yapacağımız şey suya asit
çözeltisi eklemek olacaktır. Bunu yaparken elimizde kesinlikle pH değişimlerini
takip edebileceğimiz bir pH metre olmalı. pH kağıtları da yararlı olabilir
ancak hassasiyet bakımından düşük olduklarından pH metre kadar iyi sonuç
vermeyeceklerdir. Sonuç olarak bir şekilde pH değişimlerini takip etmek
durumundayız.
1. pH beklediğimizden/arzu ettiğimiz değerden çok yüksek
ise:
Bu durumda baz kullanarak yapılan düzeltmeyi, asit stok çözeltisi kullanarak yapacağız. Asit stok çözeltisi için sülfürik asit, fosforik asit, asetik asit veya hidroklorik asit kullanılabilir. Peki bu asitleri nereden bulacağız. Sülfürik, fosforik ve hidroklorik asitler konsantre olarak satılmaktadır. Konsantre derken tehlikeli değerlerden bahsediyoruz. Olur da bu konuda bilgi ve tecrübeniz var ise, konsantre asitten 1 molar stok çözelti hazırlayarak kullanabilirsiniz. Ancak tekrar dikkat çekmek isterim ki, piyasada satılan bu asitlerin herhangi bir şekilde vücutla teması, 1. derece yanıklara sebep olacaktır. Bu sebeple bu asitlerin temin edilip kullanılmasını tavsiye etmiyoruz. Ancak bir şekilde düşük konsantrasyonlu çözeltilere erişebiliyorsak pH metre ile takip ederek pH değerini aşağı çekmede kullanabiliriz. Bu asitlere alternatif olarak asetik asit kullanılması çok daha az tehlikelidir. Ayrıca asetik asit yukarıdaki asitlere kıyasla tampon kapasitesi oluşturabildiğinden, kullanımı daha yararlı olacaktır. Asetik asidi basitçe katı limon tuzu kristalleri olarak marketten temin edebiliriz. Bu kristaller 500 ml su içeren bir pet şişe içerisinde bir 10-15 gram koyulacak şekilde çözülür ve stok çözelti hazırlanır. pH metre ile takip ederek, yukarıda pH artırmada açıkladığımız şekilde bu stok çözelti pH düşürmek için kullanılabilir.
GH değerini düşürmek
GH değerini düşürmek için yapılacak olan şeyler ihtiyaca göre, yukarıda açıkladığımız ters ozmos işlemi veya tortu alma işlemidir. Piyasada genel olarak 2 çeşit su arıtıcı bulunmaktadır:
İlki, sudaki tortuyu, bazı organik maddeleri
ve bazı iyonları tutabilen artıma sistemleridir. Bu gibi sistemlerde, su ilk
olarak çeşitli geçirgenlikte mikron filtre/filtrelerden geçirilip tortudan
ayırılır. Mikron filtreler tek kullanımlıktır ve yaklaşık altı aylık
periyotlarla değiştirilmeleri gerekir.
Ardından karbon filtreden geçirilen su, suya
renk veren ve karbon yüzeye ilgi duyan organik maddelerden arındırılır. Karbon
filtre de tek kullanımlıktır ve yüzeyi doldukça (yaklaşık 6 ay) değiştirilmesi
gerekir.
Bundan sonra sıra, sudaki kalsiyum ve
magnezyum iyonlarını filtreleyen iyon değişim filtresine gelir. Bu filtrede
bulunan polimerik malzeme, üzerinde bulunan sodyum iyonları ile kalsiyum ve
magnezyum iyonlarını yer değiştirtir. İlk iki aşamada GH bir miktar düşer ancak
iyon değişim filtresinde amaç suyu kalsiyum ve magnezyumdan arındırmak
olduğundan GH düşmez, aksine artar. Bu artışa sebep bir kalsiyum veya kalsiyuma
karşılık iki sodyum çıkışı olmasıdır. İyon değişim filtreleri, belli
periyotlarla (6 ay) çok yoğun tuzlu su çözeltilerine yatırılarak yeniden
kullanılabilir hale getirilebilir.
İyon değişim filtresinin ardından, eğer
sistemde mevcutsa sıra su tatlandırma filtrelerine gelir. Bu üç aşamanın
ardından gelen filtreler yine GH artışına sebep olur. Artışın sebebi suyun
tadını içilebilir hale getirmek için eklenen bazı organik bitkisel
iyon/maddelerdir.
Toplamak gerekirse, bu tür su arıtma sistemleri
GH değerini ancak bir miktar düşürebilir. Asıl amaç suyu insan metabolizmasına
uygun hale getirmek olduğundan, su temizlenir, saflaştırılmaz.
İkinci metod ise ters ozmos sistemler
kullanmaktır. Su arıtıcılarla aynı olarak ters ozmos sistemlerde de ilk iki
aşama mikron filtre ve karbon filtredir. Üçüncü aşama ise iyon değişim
filtresinden farklı olarak membran filtredir. Yukarıda bulunan açıklamada ve
grafik 3’te belirtildiği gibi membran filtre sudaki tüm iyon ve tortuyu, ters
ozmos işlemi ile atık olarak ayırırken temiz su çıkışından saf suya yakın su
verir. Ters ozmos sistemlerde mikron ve karbon filtre kullanılmasının amacı
membran filtrenin ömrünü uzatmaktır. Tek başına kullanıldığında çok hızlı
şekilde tıkanacağından, membran filtreden önce mikron ve karbon filtre
kullanılır. Membran filtreler tek kullanımlıktır ve 2 yıla kadar işlevini
yerine getirebilmektedir. GH değerini düşürmek için asıl etkili yöntem,
açıklamalardan da anlaşılabileceği üzere ters ozmos sistemlerdir. Ancak burada
dikkat edilmesi gereken husus, ters ozmos sistemlerde bu üç filtrenin
kullanılması gerektiğidir. Çünkü membran filtre çıkışına bağlanan filtreler
suya iyon/madde vermeyi amaçladığından GH değerini artırıcı etki oluşturacaklardır
ve akvaryum kullanımında gereksizlerdir. Ayrıca membran sonrası filtrelerin
kullanımı gereksiz yere ek maliyetler oluşturacaktır.
KH değerini düşürmek
GH’a benzer şekilde KH değerini düşürmek için de yukarıdaki metodlar kullanılabilir. Aynı şekilde ters ozmos KH düşürmede etkilidir. Suyu kaynatarak, karbonat iyonlarını karbondioksit gazına dönüştürerek de KH düşürülebilir ancak bu yöntem çok çok pahalı olacaktır.
KH değerini artırmak
KH değerini artırmak için basitçe suya karbonat eklenmelidir. Arzuya göre bir TDS metre kullanarak istenen miktarda karbonat eklenebilir ve KH artırılabilir.
Suya Karbondioksit gazı (CO2)
eklemek
Bitkili akvaryumlarda, karbondioksit fotosentez için gerekli bir bileşendir ve bitkilere karbondioksit sağlanmalıdır. Ancak CO2 kullanımı bir zorunluluk değildir ve dikkatli olunmalıdır. Tankta az miktarda bitki ve kıyasla fazla miktarda canlı var ise CO2 kullanımına ihtiyaç olmayabilir. Böyle bir durumda suya CO2 eklenmesi pH’ı aniden çok düşük değerlere çekebilmekte, bu durumda bitkilerin yanmasına neden olabilmektedir. Ayrıca doğada, bitkilerin bulunduğu habitatlar akvaryumda sağlanan miktarda CO2 içermez. Normalden bir miktar fazla CO2 eklenmesi fotosentezi, dolayısıyla gelişim hızlandırır ancak ekleme yüksek miktarlarda yapılmamalıdır. Karbondioksit kaynağı olarak pet şişede mayalı sistemler, piknik tüpü veya yangın tüpünde mayalı sistemler olduğu gibi karbondioksit tüpleri de kullanılmaktadır. Aşağıdaki linkte, piknik tüpü ile DIY piknik tüplü mayalı sistem yapım aşamaları mevcut.
Bitkili akvaryumlarda iyon gereksinimleri
Tatlı su bitkileri sağlıklı gelişim gösterebilmek için potasyum, fosfat, nitrat ve çeşitli eser elementlere ihtiyaç duyarlar. Doğada bu ihtiyaçlarını, nehirlerin alüvyonları çözerek taşıması ile karşılayabilen bitkiler, akvaryumlarda kısıtlı miktarda iyona erişebilirler. Ayrıca her türün iyon gereksinimi ve iyon emilim hızı farklılık göstereceğinden, suda bazı iyonlar, bitki türleriyle ilişkili olarak daha hızlı tükenir. İyon eksikliği dolayısıyla bitkilerde çeşitli form ve renk bozuklukları meydana gelebileceği gibi yapraklarda delikler ve gelişimin durması da gözlenebilir. Bu duruma çözüm olarak suya iyon takviyesi yapılabilir. Ancak bunu yaparken kullanılan iyonların içerik ve miktarları iyi tahlil edilmelidir.
Bahçe bitkilerinden hatırlanacağı gibi, çok
yüksek miktarda veya dengesiz besin eklemek, bitkilere faydadan çok zarar
verecektir. Bu durum akvaryum bitkilerinde daha hassastır. Akvaryum bitkilerinin
gelişimleri, 500ppm üzeri sertlikte sularda durmakta, daha sert sularda
çürümeler başlamaktadır. Ayrıca pH 5.0 ve altında aynı şekilde bitkilerin
hayatta kalması mümkün olmamaktadır. Tüm bu sorunlara ek olarak, akvaryum bitkilerinde,
dengesiz besin takviyesi neticesinde yosun oluşumları gözlenmektedir. Sakal
yosunundan yeşil alge kadar pek çok yosun türü, suda hazır halde bulunan eser
element ve aminoasitler yardımıyla hızlı gelişim gösterir. Yosun türleri
primitif canlılar olduklarından, suda serbest halde bulunan vitamin ve
aminoasitleri bitkilerden çok daha hızlı kullanarak, bitkilerden daha hızlı
gelişim gösterirler. Bu durum, bitkiler için sağlanan yararlı iyonların yosunlar
tarafından tüketilmesine, dolayısıyla bitkilerin de besinsiz kalarak
gelişimlerini durdurmalarına neden olur. Bu sebeple aminoasit ve vitamin içeren
bitki besinleri, akvaryum bitkilerinde yosun gelişimini tetikleyici etki
gösterirler ve bitkiler için sağlanan iyonların yosunlar tarafından
tüketilmesine yol açarlar. Bu tür besinlerin kullanımından kaçınılmalıdır.
Bitkili akvaryum suyunda gereksiz,
zararlı ve zararsız iyonlar
Şebeke suyunda bulunan pek çok iyon bitkili akvaryum kullanımı için gereksizken, bazı çeşitler de zararlıdır.
Örneğin şebeke suyu dezenfeksiyon amaçlı
olarak yüksek miktarda klor iyonu
içerir. Klorun akvaryum canlıları için yararlı bir etkisi bulunmamakla birlikte
fazlası zararlıdır. Gereken doz halihazırda yemlerden veya suda arta kalan
klordan sağlanacağı için klorun arıtılması yararlıdır. Hobiciler klordan
kurtulabilmek için, genelde suyu havalandırma yoluna başvururlar. Dinlendirilen
(açık havada bekletilen) veya havalandırılan suda, iki klor iyonu bir araya
gelerek klor gazını oluşturur. Oluşan klor gazı, suda çözünürlüğü çok düşük
olduğundan uçar ve su klordan arındırılır. Ancak bu tepkime belirli bir
seviyeye kadar gerçekleşeceğinden suda yine belli bir miktar klor kalır.
Klordan kurtulmanın en etkili yolu ters ozmos yöntemidir.
Sodyum şebeke suyunda fazlaca bulunan ancak bitkiler veya
canlılar üzerinde zararlı etkisi bulunmayan bir iyondur. Arıtılmasının yarar
sağlayabileceği gibi arıtılmadan kullanılmasının doğrudan bir zararı
olmayacaktır.
Sülfat iyonu pek çok pozitif yüklü iyonun anyonu olarak suda
bulunur ancak canlılar veya bitkiler üzerinde zararlı etkisi yoktur.
Bakır iyonu bitkiler için gerekli iyonlardan birisidir. Ancak
bitkiler bu iyona yüksek konsantrasyonlarda ihtiyaç duymadıklarından, yemler vs
vasıtasıyla sağlanması yeterlidir. Bakır gereğinden fazla miktarda
kullanıldığında zararlı etki ortaya çıkarmaktadır. Oksidasyon değerindeki farklılıklar
neticesinde, bitkilerde ve özellikle omurgasız canlılarda inhibite etki
gösterebilmektedir.
Amonyak canlı dışkılarının ilk ürünü olarak ortaya çıkabilen ve
canlılar üzerinde zararlı etki gösteren bir iyondur. Filtrasyon kabiliyeti
yüksek akvaryumlarda çok hızlı olarak oksitlenerek nitrit ve nitrata
dönüştürüleceğinden zararlı etkisi düşürülmüş olur. Canlı yükü yüksek ve
filtrasyonu zayıf akvaryumlarda bitkiler üzerinde doğrudan ve çok zararlı etki
gösterir.
Üre akvaryumda olmaması gereken bir azotlu atık bileşiğidir.
İşlenip zararsız formlara dönüştürülmesi zahmetli olan bu bileşiğin akvaryuma
eklenmesi bitkilere doğrudan zarar verir. Azot kaynağı olarak üre içeren bitki
besinleri kesinlikle akvaryuma eklenmemelidir. Zirai azot ve nitrat
gübrelerinde üre bulunduğu için akvaryumlarda kullanılmasından sakınılmalıdır.
Hidrojen Peroksit kimi hobiciler tarafından yosun kurutucu
olarak akvaryumda kullanılmaktadır. Ancak bu bileşik bir radikalik başlatıcıdır
ve akvaryumdaki canlılar için zararlıdır. Etkileşimde bulunduğu tüm hücreleri
öldürür. Yosunların kurutulmasında kullanılmasının nedeni, yosunların,
bitkilere kıyasla daha basit yapıda olmalarıdır. Yosunlar etkileşim sonrası
hayatta kalabilecek güçte olmadıklarından kururlar ancak bitkilerin yalnızca
bazı hücreleri ölür. Kalan hücreler yeniden gelişim gösterdiğinden hayatta
kalır. Ancak balıklara veya omurgasızlara temas durumunda en iyi ihtimalle
canlı üzerinde yaralar oluşturacaktır. Kullanımı tavsiye edilmemektedir.
Elimden geldiğince su değerlerini ifade eden
kavramları açıklamaya çalıştım. Eksik kalan noktalar üzerinde, bu başlık
altında tecrübeli hobiciler ile bilgi paylaşımı yapmaya devam ederiz umarım.
Saygılar, sevgiler…
Beğenenler: [T]164416,fth0507[/T][T]8082,alperozoglu[/T][T]69574,fantastik3[/T][T]274276,yigidoumit[/T]
Teşekkür Edenler: [T]164416,fth0507[/T][T]8082,alperozoglu[/T][T]69574,fantastik3[/T][T]274276,yigidoumit[/T]
+1: [T]274276,yigidoumit[/T]
Üye imzalarını sadece giriş yapan üyelerimiz görebilir
Üye imzalarını sadece giriş yapan üyelerimiz görebilir
Üye imzalarını sadece giriş yapan üyelerimiz görebilir
Üye imzalarını sadece giriş yapan üyelerimiz görebilir